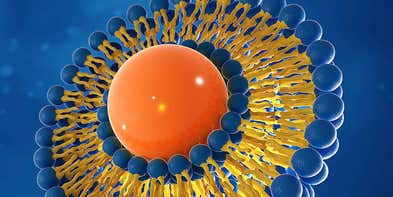

製剤処方開発を促進する物理化学分析ソリューションと専門知識を備え、バイオアベイラビリティと加工要件に適合

医薬製剤の開発は,新薬の発見と市販の医薬品開発の成功を結びつけるものです。処方開発の科学者は、患者のニーズに基づいて効果的な薬物送達を実現するための最適な経路を決定してから、製剤のバイオアベイラビリティとプロセス要件に関する知識に基づいて処方の特性を最適化する必要があります。
これは難しい課題です。 前臨床処方開発における新製剤のうち、市場に到達できるものは10%にすぎません。 医薬品開発のコストが上昇し、創薬パイプラインの価値を解放する圧力も高まっていることから、先発医薬品開発企業は、効果的な処方選択を迅速化する方法を見つけるために多大な努力をしています。 薬剤原料と製剤の形態と構造を完全に理解することが、これを実現する上で重要であると考えられています。
ジェネリック医薬品企業にも同様の課題があり、そこでも複雑な製剤処方の開発を成功させるのは依然として大変なことです。 新しい複雑なジェネリック医薬品には、未開発の市場が大きく存在します。 世界の規制当局の指導により、複雑な投与形態のミクロ構造に関する物理化学的詳細を理解することが製品開発の成功につながることが認識されるようになりました。
マルバーン・パナリティカルの物理化学技術は、これらの処方の課題に対処するために日常的に応用されています。 当社のソリューションは、物理化学的特性を特徴付け、原薬と医薬品の形態をよりよく理解し、賦形剤の選択を支援し、製剤内の賦形剤の機能を理解し、保管または処理が医薬品の性能にどのように影響するかを評価するために使用されます。当社の専門知識により、適切なデータを提供し、製剤開発の成功を引き出す洞察を提供します。


製剤処方の開発を成功させるには、原薬(API)と不活性型賦形剤を組み合わせる必要があります。 賦形剤は単純な増量剤であり、統合含量均一性を制御するために設計されています。 しかし、薬剤の放出を制御したり、薬剤が目的の作用部位に到達するようにしたりする上で、いくつかの賦形剤が機能的な役割を果たすようになってきています。 ここでは、必要な治療時間枠内に正しい投与量が実現されるようにするため、選択した賦形剤と製剤原料との適合性がとても重要です。 物理化学分析は、賦形剤の選択を支援し、製剤原料と製剤の安定性の評価を可能にするとともに、処方性能に関係する重要材料特性(CMA)を設計領域定義の一部として特定し,下流工程の製造管理に適用できるようにします。
ゼータサイザーUltra は、分散性、エマルション、クリームの安定性と品質を特徴付けるために使用され、調合時間を短縮し、新製品の発売までの時間を短縮することができます。
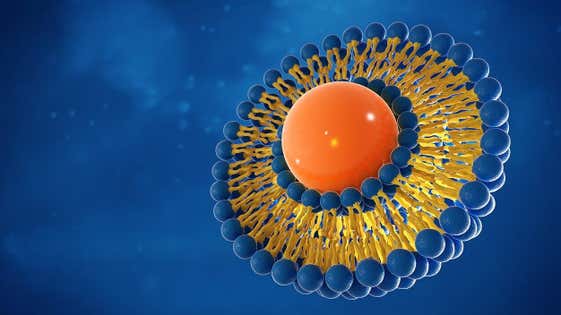
再現性のある薬物送達を達成するための要件が複雑になっていることは、処方開発の科学者にとって共通の課題となっています。 多くの新しい原薬(API)は不溶性であり、従来の経口固形薬送達は不適切になりました。 そのため、処方の複雑さは増大しており、経口投与のバイオアベイラビリティを向上させるか、作用部位の薬物濃度が治療要件を満たすように局所的に投与できるようにするかのいずれかが求められます。
リポソームやその他のナノ粒子デリバリーシステムをベースとした新しいドラッグデリバリーシステムがより頻繁に利用され、ドラッグターゲティングの改善に利用されるようになっています。 Malvern Panalyticalの補完的な分析技術により、処方開発者は、API、賦形剤の処方、安定性を理解できます。 これにより、複雑な処方の最適化が容易になり、効果的な処方候補を選択する時間が短縮されます。
複雑な処方の開発の課題は、ジェネリック医薬品の開発にも広がっています。 世界中の規制当局は、複雑なジェネリック医薬品の導入が成功しないことによる、医療費への影響を認識しています。 規制当局は、これに対応して医薬品固有のガイダンスを発表し、参照する医薬品(RLD)と比較した試験用ジェネリック医薬品の生物学的同等性評価の一環として、物理化学つまりQ3同等性を評価する役割を強調しました。
in vitro生物学的同等性試験法の応用には、臨床的エンドポイント研究の必要性を排除して、新しいジェネリック医薬品の市場投入までの時間を大幅に短縮する潜在性があります。 Malvern Panalyticalの物理化学分析技術および専門知識を備えたツールキットは、薬剤と薬剤処方の両方の特性の評価を可能にするもので、in vitro生物学的同等性の研究を成功させる上で重要な役割を果たします。

優れたジェネリック医薬品処方の開発は、参照する医薬品(RLD)の構造と性能を理解することから始まります。 ここでは、in vitro生物学的同等性評価と同様、物理化学分析に、製剤処方要件の理解を深める上で果たす重要な役割があります。 RLD医薬品内に存在するAPIおよび賦形剤の先行的、定量的、構造的、形態学的特性評価により、処方最適化のプロトタイプを作成し、開発リスクを大幅に低減できます。
この脱処方アプローチのメリットは、ジェネリック医薬品の企業に限られるものではありません。 新製剤の開発・製造にも同様の方法を適用することで、スケールアップ中の処方性能の変化の根本原因を特定するのに役立つ知見が得られます。 また、製造プロセスや製造場所に対するマーケティング後の変更が、製剤の性能に与える影響を企業が理解するのにも役立ちます。
モフォロギ4-ID を使用して変形の課題を単純化して解決し、in vitro法による生物学的同等性を確立することができます。 また、製造中に異常、異物を検出し、プロセス偏差を特定することもできます。