단백질 안정성의 신뢰성 있는 특성 분석
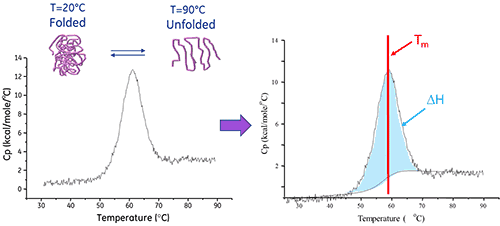
시차 주사 열량측정법(DSC)은 기본 형태의 생체 분자 또는 단백질의 안정성을 직접 특성화하는 데 사용되는 분석 기법입니다. 일정한 속도로 가열되면 분자의 열적 변성과 연관된 열 변화를 측정하여 이러한 분석을 수행합니다.
용액 내 생체 분자는 네이티브(접힌) 형태와 변성된(풀린) 형태 간에 균형을 이루고 있습니다. 열 전이 중간점(Tm)이 높을 수록 분자가 더 안정적인 상태가 됩니다. DSC는 열 유도 변성으로 인한 풀린 형태의 엔탈피를 측정합니다. 또한 변성에 대한 열용량(ΔCp) 변화를 측정하는 데 사용됩니다. DSC는 네이티브 생체 분자의 안정성과 접힘에 기여하는 요소를 해석합니다. 이 요소에는 소수성 상호 작용, 수소 결합, 구조적인 엔트로피(conformational entropy) 및 물리적 환경이 포함됩니다.
DSC에서 확보한 정확한 고품질 데이터는 잠재적인 치료 후보 물질의 처방과 공정 개발에서 단백질 안정성에 대한 필수 정보를 제공합니다.
단백질, 핵산 및 지질과 같은 거대분자 및 거대분자 어셈블리(>5000 돌턴)는 열적으로 유도된 구조적 변화를 겪는 명확한 구조를 형성할 수 있습니다. 구조적으로 재배열되면 비공유 결합의 재배치에 의해 열 흡수가 이루어집니다. 시차 주사 열량측정계는 열 흡수량을 측정합니다.
DSC 시스템의 열 중심부는 기준 셀과 시료 셀 등 두 개의 셀로 구성됩니다.
이 장치는 두 셀이 가열됨에 따라 동일한 온도로 유지되도록 설계되었습니다.
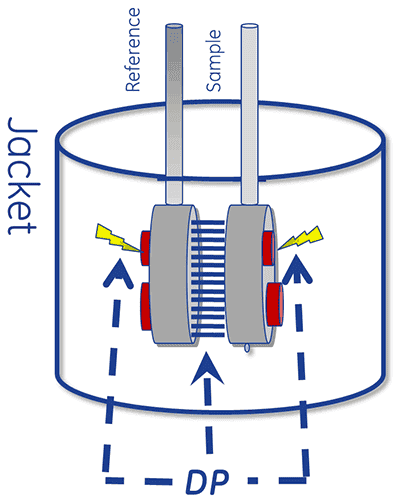
DSC 측정을 수행하려면 기준 셀은 완충액으로, 시료 셀은 시료 용액으로 채웁니다. 이 셀들은 일정한 주사 속도로 가열됩니다.
단백질 풀림이 셀 간의 온도차(ΔT)를 유발하면 열 흡수로 인해 펠티에 장치에서 열 구배가 형성됩니다. 이렇게 하면 전압이 설정되어 전력으로 변환되고 펠티에 장치를 제어하여 ΔT(온도차)를 0°C로 되돌리는 데 사용됩니다. 또한 이 셀은 전도를 통해 수동으로 열 평형 상태에 도달할 수 있습니다.
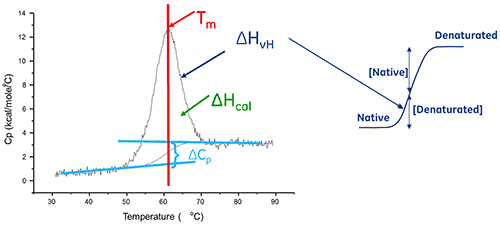
단백질 풀림의 엔탈피는 농도 정규화 DSC 피크 아래에 있는 영역으로, 몰당 칼로리(또는 줄) 단위가 사용됩니다.
어떤 경우에는 열역학적 모델을 데이터에 맞추어 조정하여 기브스 자유 에너지(Gibb's free energy, ΔG), 열량 측정 엔탈피(calorimetric enthalpy, ΔHcal), 반트 호프 엔탈피(van't Hoff enthalpy, ΔHvH), 엔트로피(ΔS) 및 전이와 연관된 열용량 변화(ΔCp)를 확보할 수 있습니다.
시차 주사 열량측정법 분석은 신약 발견 및 개발에 널리 사용됩니다. 대표적인 응용 분야로 다음과 같은 예를 들 수 있습니다.

MicroCal PEAQ-DSC Automated통제된 환경을 위한 절대적 기준의 단백질 안정성 분석 |

MicroCal PEAQ-DSC연구 응용 분야를 위한 절대적 기준의 단백질 안정성 분석 |
|
|---|---|---|
| 측정 유형 | ||
| 비표지(label-free) 분석법 | ||
| 단백질 안정성 | ||
| 기술 유형 | ||
| 시차 주사 열량측정법(DSC) | ||
| 샘플 처리량 | ||
| 온도 범위 | ||