通常、バクテリオファージおよびウイルス粒子の滴定量はプラーク法で、動物細胞のウイルスの場合は細胞を用いる生物検定で確立されます。 これらのアレイシステムでは、感染性のウイルス粒子が集密的な細胞層で成長してプラーク(破壊された細胞の帯域)を生成します。これを計数して、プラーク形成単位(pfu)を決定できます。 この方法では、感染性のウイルス粒子を直接計数できますが、非感染性のウイルス粒子はプラークを生成せず、多種類のウイルス粒子を含む凝集体から単一のプラーク数のみが得られることになります。 メーカーは多くの場合、標本に含まれるウイルスの粒子数、感染性であるかどうか、および該当する場合は標本での凝集の進行程度(期限付き保存期間の初期指標)を知る必要があります。
ナノ粒子トラッキング解析(NTA)では、液体中にあるウイルスやウイルス凝集体などのナノ粒子をリアルタイムで直接および個別に視覚化でき、高分解能の粒度分布プロファイルを得ることができます。 この手法は高速で信頼性が高く、正確で低コストであることから、動的光散乱(DLS)、光子相関分光法(PCS)、電子顕微鏡法(EM)などの既存のナノ粒子分析法を補完する魅力的な手法です。
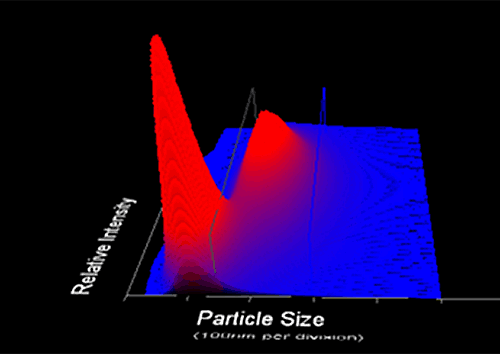
マルバーンのナノサイト製品は、NTAを使用して液体中に存在する直径10~2000 nmの粒子を解析します。 NTAでは、懸濁液中の粒度分布を得るために、光散乱法とブラウン運動の両方の特性を使用します。 レーザー光が試料チャンバーを通過し、懸濁液中の光路に存在する粒子が光を散乱するので、それらの粒子を簡単に視覚化できます。 その後、ストークス - アインシュタインの式を使用して、個々の粒子径が計算されます。 結果は、個々の粒子の径と数のグラフ(または粒子径と 相対輝度)のグラフとして表示されます。
|
ウイルスワクチンの製剤では、安定であること、および既知の割合で活性要素が含まれていることが実証(検証)されている必要があります。 NTAを使用すると、製品の純度と濃度を即座にまた直接推定できます。 同様に、ウイルス標本における凝集体形成の程度と速度もNTAで測定できるので、メーカーはさらに優れた製品製造プロセスを開発したり、製品の保存期間を長くしたりできます。
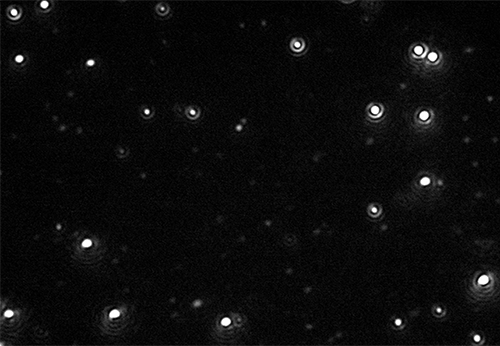
NTAでは標本に含まれるすべての粒子を視覚化して粒子径を測定できるので、ナノ粒子の含有物に関する追加情報を従来のTCID50やプラーク法よりも短時間で得ることができます。 例えば、大きい粒子の存在(NTAで粒子径の測定と計数の両方が可能)は、細胞培養プロセスによる非ウイルス由来の細胞破片である場合も、多数のビリオンを含むウイルス粒子の凝集体である場合もあります。
いずれの場合でも、このような凝集体/異物粒子はメーカーにとって問題となる可能性がありますが、マルバーンのナノサイトシステムで即座に識別できます。
|
Virus clearance effectiveness is assayed by spiking samples with carefully prepared high titer virus samples (of various types depending on application). 次に、これらのウイルススパイクを使用して、クリアランス手順として適合する必要がある処理手順が検証されます。 データの収集には、純度が高く凝集のないウイルススパイク試料を使用する必要があり、これらの試料はまず高滴定量で調整し、使用前に保管する必要があります。 NTAは、保管前後の凝集状態の確立に理想的です。
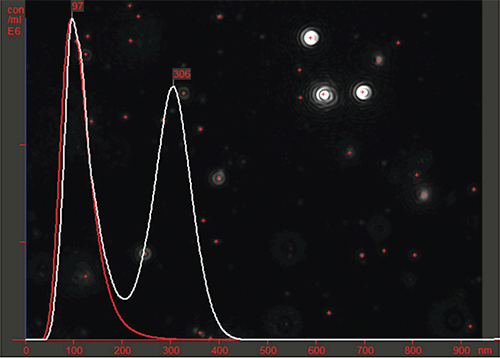
マルバーンのナノサイト装置シリーズが持つ、ウイルス標本に異物粒子や凝集体が含まれる程度を短時間で確立する機能、およびその程度を定量する機能は、ウイルス標本の精製プロトコルの最適化に関心を持つプロセス開発者にとって非常に貴重であることが実証されています。 例えば、図3に、部分的に精製したウイルス標本(白線)と、同一サンプルに異物粒子や凝集体をすべて効率的に除去する精製プロトコルを実施したもの(赤線)の差を示します。 縦軸は粒子濃度(ウイルス粒子数/mL)を表すことに注意してください。
|
NTAを使用するウイルス粒子の検出と計数は、ストラスクライド大学の薬理生物医学研究所(IPBS)で研究者に重要な情報を提供しています。 この研究所のチームは、自然に発生するバクテリアを使用してMRSAを撃退する手法を開発しました。 MRSA(メシチリン耐性黄色ブドウ球菌)は細菌である黄色ブドウ球菌の一種で、ほとんどの抗生物質への耐性を獲得しており、治療が困難で死亡に至る可能性があります。 この抗生物質への耐性を持つ細菌は洗剤で殺すことができますが、洗剤の希釈と塗布が多くの場合に一貫しておらず効果が得られないため、バクテリオファージセラピーが魅力的な代替手段です。 バクテリオファージセラピーでは、宿主菌内部で増殖してから宿主細胞を溶解するバクテリオファージを使用して、宿主菌を破壊します。
Mike Mattey博士(IPBSの名誉講師)が率いるチームでは、 バクテリオファージ培養物の特性評価にNTAが使用されています。 細菌が侵入する危険が高いサイト(縫合部、器具、および創傷)に乾燥被膜としてバクテリオファージを配置する前に、この培養物の特性と濃度を評価する必要があります。 NTAにより、チームはウイルス培養物の表示と粒子径測定を即座にリアルタイムで、また低コストで行うことができます。 「ウイルス母集団の特性を評価するには、20~1000 nmの範囲の凝集を評価する必要があります」 とMattey博士は語っています。 「ナノサイトを使用すると、試料の定量的特性評価を短時間で簡単に行うことができます。 さらに、ナノサイトの技術が提供する信頼性の高い粒子母集団の表示は、計数結果の裏付けになります。」
これまで解析に成功した各種ウイルスの一部を示します。
(Carr, B. (2009)Nanoparticle tracking analysis: direct visualization for counting and characterizing virus particles in liquids, Meeting the challenge of viral pandemics, 2009 - biotech-online.com)