이 응용 노트에서는 약물 전달 나노 입자의 크기 및 농도 측정을 위한 나노 입자 추적 분석(NTA)의 활용에 대해 설명합니다. 추가적으로 형광 표지 약물 분자를 사용하여 얼마나 많은 약물 전달 나노 입자가 약물 분자에 성공적으로 봉입되었는지에 대한 측정이 가능하였습니다.
지난 20여년간 전세계적 수준의 생체의학 연구는 나노 입자 기반 약물을 개발하고 이를 실험실에서 실제 임상용으로 전환하기 위해 수많은 노력을 기울이고 있습니다.
오늘날 많은 고단백 분자 기반 약물이 저용량(독성으로 인해) 또는 특정 기관, 세포 유형 등에 대한 표적화 효율의 부족과 같은 준최적 조건에서 사용됩니다.
최근 연구에 의하면 고분자 또는 리포좀과 같은 나노 입자가 이러한 문제들 중 일부를 해결할 수 있는 약물 전달체로서 우수한 특성을 가진 것으로 밝혀졌습니다. 나노 입자 기반 약물 고려 시 약동학 또는 인체 내 표적에 도달하는 효율 및 능력에 상당한 영향을 미치기 때문에 이들 벡터의 크기에 대한 특성 분석이 매우 중요합니다. 이와 마찬가지로 중요한 점은 나노 물질의 농도뿐만 아니라 특히 관심 약물에 봉입되는 나노 물질의 용량을 알 수 있어야 합니다.
여기서는 약물 전달 나노 입자의 크기 및 농도 측정을 위한 나노 입자 추적 분석(NTA)의 활용에 대해 설명합니다. 추가적으로 형광 표지 약물 분자를 사용하여 얼마나 많은 약물 전달 나노 입자가 약물 분자에 성공적으로 봉입되었는지에 대한 측정이 가능하였습니다.
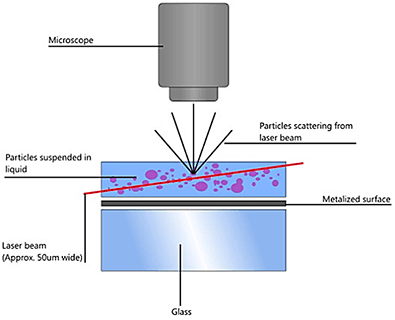
NTA에는 현탁액(liquid suspension) 내 샘플의 입도 분포를 확인하기 위해 광 산란과 브라운 운동의 속성을 모두 활용합니다. 샘플 챔버에 레이저를 통과시키면 현탁액에서 이 광선의 경로에 있는 입자가 빛을 산란시켜 카메라가 장착된 20배율 현미경으로 쉽게 시각화할 수 있습니다. 초당 약 30프레임(fps)으로 작동하는 카메라가 약 100μm x 80μm x 10μm의 시야 내에서 브라운 운동을 하는 입자의 이미지 비디오 파일을 캡처합니다(그림 A).
|
입자의 움직임이 프레임별로 캡처됩니다. 특허 받은 NTA 소프트웨어가 관찰된 입자 각각의 중심부를 동시에 식별하고 추적하며 XY 평면에서 각 입자의 평균 이동 거리를 측정합니다. 이 값을 이용하여 입자 확산 계수(Dt)를 측정하고 샘플 온도(T)와 용매 점도(η)를 알고 있다는 가정 하에 이 값을 스톡스-아인슈타인 방정식(방정식 1)에 대입하여 구형으로 가정한 입자의 유체역학적 직경(d)을 계산할 수 있습니다.
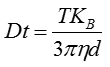
|
NTA는 많은 숫자의 입자를 종합적으로 다루는 총체적 측정 기법이 아니라 입자 하나 하나의 크기를 다른 입자의 크기에 상관없이 개별적으로 측정하는 기법입니다. NTA를 통해 작성된 입자 크기 분포 프로파일이 그림 B에 예로 제시되어 있습니다.

|
또한 정해진 관찰 영역(대략 100μm x 80μm) 내에서 약 10μm 깊이에서 레이저를 조사하는 조건 하에 입자 운동이 측정되었습니다. 이 그림을 통해 샘플의 산란 체적을 추정해 볼 수 있습니다. 관찰 영역 내에서 입자 농도를 측정하고 더 큰 체적을 추론함으로써 주어진 모든 크기 수준에 대해서나 전체 체적에 대해 mL당 입자 수 단위의 농도 추정치를 구할 수 있습니다. 마지막으로 형광 모드에서 적절하게 라벨 표시된 입자를 감별할 수 있습니다.
sCMOS 카메라, 405nm 레이저 및 430nm 장파역 통과 필터로 구성된 NanoSight LM10 HSBF 시스템을 사용했습니다. 데이터 분석에는 NTA 소프트웨어 2.3.5를 사용했습니다.
젖산 중합체(PLA) 입자(Adjuvatis)를 설계 및 합성하여 형광 표지(Coumarin6, 여기 370nm; 발광 470mm) (PLA-Coum)에 결합된 관심 약물에 봉입하였습니다.
PLA-coum 나노 입자를 무입자 초순수 물*로 100배 희석하고 피펫을 사용하여 혼합하였습니다. * 사용 전 NTA를 통해 초순수 물을 검사하였고 오염 입자가 없음을 확인하였습니다.
희석한 샘플은 1mL 실리콘 오일프리 주사기를 사용하여 레이저 샘플 챔버에 주입하였습니다.
샘플 챔버를 장비에 로딩하였습니다. 이미지는 입자가 초점에 오도록 조정되었고 광 산란(표준) 모드의 데이터 생성을 위해 60초간 카메라 레벨 7을 사용하여 비디오를 캡처하였습니다(샘플의 모든 입자가 측정됨). 샘플 챔버가 장비에 남아있는 상태에서 카메라 레벨을 최대(레벨 16)로 올리고 430nm 장파역 통과 필터 삽입 및 형광 모드 데이터 획득을 위한 초점 재조정 후 두 번째 60초 비디오를 캡처하였습니다(형광 신호를 방출하는 입자만 측정됨).
이어서 산란 모드와 형광 모드에 대해 둘 다 검출 임계값 4를 사용하여 이들 비디오를 처리하였습니다. 최소 추적 길이는 산란 및 형광 모드에 대해 둘 다 6으로 설정했습니다.
두 측정 모드에 대해 크기 분포 데이터를 획득하여 비교를 위해 중첩하였습니다.
라벨 표시 및 비표시 PLA 나노 입자의 혼합물은 샘플 생산 방법의 결과로서 예측되었습니다. 산란 모드(그림 1) 및 형광 모드(그림 2) 하에서 이들 입자에 대한 NTA 데이터를 획득하였습니다. 비디오의 프레임간 각각의 입자가 이동한 거리를 사용하여 분산 계수 및 최종적으로 입자의 크기를 생성하였고(그림 1b 및 그림 2b), 반면에 비디오의 각 프레임 내에 있는 평균 입자수를 사용하여 샘플 농도를 추정하였습니다(그림 1a 및 그림 2a). 이들 매개 변수를 사용하여 각 측정 모드에 대한 크기 분포 프로파일 그래프를 생성하였습니다(그림 1c 및 그림 2c). 크기 및 농도에 대한 요약 데이터가 표 1과 표 2에 나와 있습니다.

|

|
|
| 평균: | 214nm |
| 모드: | 199nm |
| 측정 농도: | 1.23 x 109입자수/mL |
| 희석 인자: | 100배 |
| 최종 농도: | 1.23 x 1011입자수/mL |
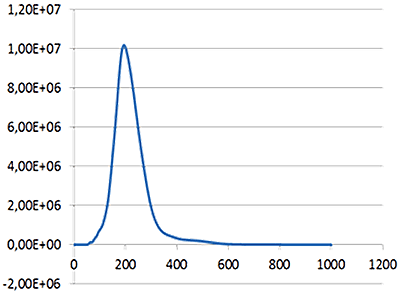
그림 1a에서는 산란 모드에서 볼 수 있는 샘플을 보여줍니다. 브라운 운동으로 움직이는 입자는 NTA 2.3.5 소프트웨어를 사용하여 추적하였고(그림 1b) 샘플 농도도 추정하였습니다. NTA를 통해 비디오의 프레임간 입자 이동을 추적하여 각 입자에 대한 확산 계수를 계산하고 고분해능의 크기 분포 프로파일을 제공해 줍니다(그림 1c) (x축 = 반경(nm), y축 = 농도(mL당 입자수)). 크기 및 농도 데이터 요약은 표 1에 나와 있습니다.

|
|
|
| 평균: | 259nm |
| 모드: | 223nm |
| 측정 농도: | 5.31 x 108입자수/mL |
| 희석 인자: | 100배 |
| 최종 농도: | 5.31 x 1010입자수/mL |
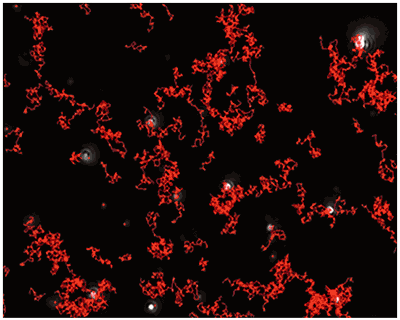
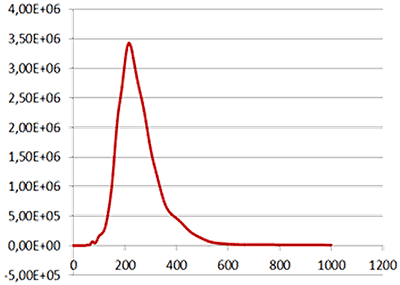
그림 2a에서는 형광 모드에서 볼 수 있는 샘플을 보여줍니다. 430nm 장파역 통과 필터를 통해 측정한 샘플을 사용하였으며, 표시된 입자만 추적하였습니다(그림 2b). Stokes-Einstein 방정식을 사용하여 입자의 브라운 운동으로부터 획득한 확산 계수에서 입자 크기를 유도하였습니다. 각 프레임 내 평균 입자수를 통해 입자 농도를 추정할 수 있습니다(그림 2a). 크기 분포 프로파일은 그림 2c에 표시되어 있습니다(x축 = 반경(nm), y축 = 농도(mL당 입자수)). 크기 및 농도 데이터 요약은 표 2에 나와 있습니다.
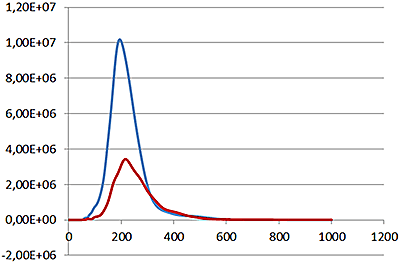
산란 모드(필터 없음)에서의 샘플 분석(그림 3 파란색 선)은 1.23e+11입자수/mL의 최종 농도와 함께 199nm에서의 모달 분포를 보여줍니다. 형광 모드(430nm 장파역 통과 필터 삽입)에서 라벨 표시 모집단의 분포(그림 3 빨간색 선)는 5.31e+10입자수/mL의 최종 농도와 함께 223nm에서 약간 더 큰 모드를 보여줍니다. 분포의 폭은 서로 유사했습니다. 또한 샘플은 확인된 후속 피크가 없으므로 단분산성이 있는 것으로 나타났습니다.
이들 데이터는 PLA 입자가 형광 표지 약물 분자에 봉입되었을 때 잠재적으로 평균 10% 더 크다는 것과 40%를 넘는 약물 전달 PLA 입자가 약물 분자에 성공적으로 봉입되었음을 나타냅니다.
|
산란 모드(파란색 선) 및 형광 모드(빨간색 선)에서 PLA-coum 나노 입자에 대한 크기 분포 프로파일의 중첩(x축 = 반경(nm), y축 = 농도(mL당 입자수))
NanoSight NTA 측정을 통해 젖산 중합체 나노 입자의 크기와 농도에 대한 신속한 평가를 수행하였습니다. 형광 표지 약물 분자로 봉입되면 형광단이 들어있는 입자의 부분 모집단은 전체 모집단으로부터 구별할 수 있게 되며 이는 봉입 공정 효율에 대한 중요한 정보를 제공해 줍니다. 이들 데이터는 약물 전달 연구자들에게 시간과 노력을 절약해 주면서 빠르고 쉬운 방법으로 개선된 봉입 공정을 확인하는 데 사용할 수 있습니다.