단백질 상호작용은 정전기력에 강한 영향을 미친다. 수소결합과 런던 힘은 위치와 배향을 나타내는 중요한 요소인 동시에 표면전하의 접근을 컨트롤하는 원거리의 정전기적 상호작용이다. 단백질 표면 전하밀도나 표면 전위보다는 실질적으로 정전기적 상호작용을 조정하는 힘은 미끄럼면 에서의 제타전위이다.
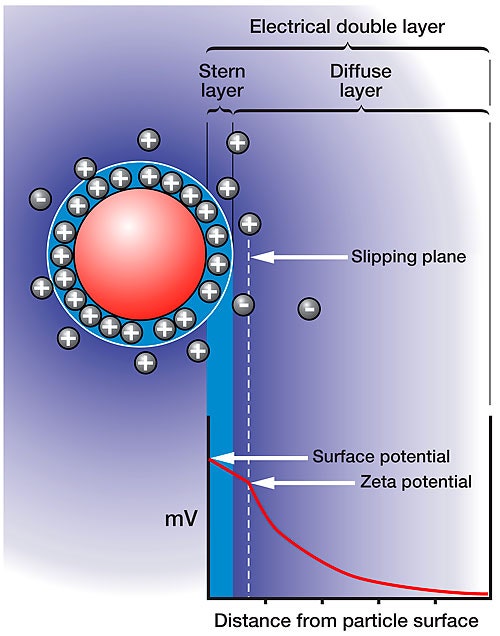
그림 1 은 용액 안에서의 하전입자 주위의 이온들의 분포를 세부적으로 나타내었다. 하전입자의 표면에 가장 가까운 층은 응축되거나 흡수된 카운터 이온들로 이루어져 있다. 이 층의 바깥 경계는 고정층으로 정의된다. 두번째 층은 분산된 하전입자의 이온들로 구성되어 있다. 이 확산 층 내에서 개념적인 경계는 이온 입자가 이동하면 입자와 함께 이동하는 구간입니다. 이 층의 바깥 경계는 미끄럼면으로 정의되고, 정전기적 상호작용의 힘으로 정의되는 미끄러지는 경계 안에서의 표면전하, 흡수된 이온 및 분산된 이온 전하들의 합이다. 이러한 미끄럼면에서의 전하나 전위 포텐셜은 제타전위로 정의된다.
|
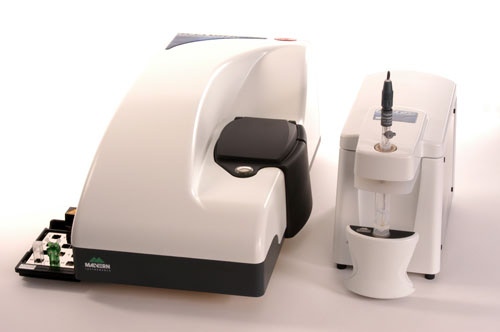
Zetasizer 나노시스템은 단백질 샘플 분석에 적합한 정적광산란, 동적광산란 및 전기영동광산란의 조합으로 이루어진 이상적인 장비이다. 나노시스템은 크기와 분자량, 그리고 제타전위를 측정한다. 특히 낮은 샘플 볼륨과 고감도가 필수적으로 요구되는 단백질 분석 관련분야의 응용을 위해 특별히 디자인되었다. 나노 시스템과 자동화된 pH, 첨가물, 희석, 전도도을 용이하게 할 수 있는 MPT-2 로 자동 측정이 가능하다.
소 혈청 알부민(BSA: Bovine serum albumin)은 100 mM NaCl 과 pH11 로 조정된 1mg/ml 의 농도로 시료를 0.1μm Anotop 필터를 통하여 여과되었다. 10ml 의 시료는 0.5M HCl, 0.1M HCl, 그리고 0.5M NaOH 의 적정제로 전처리 한후 Zetasizer Nano MPT-2 시스템의 시료용기에 주입했다. 시료는 0.5 pH 단위로 증가시켜 pH 2 부터 적정하였다. 주목할만한 것은 본 실험은 10 ml 의 시료를 사용하지만 MPT-2 장비는 3ml 이하의 시료 적정으로 충분하다.
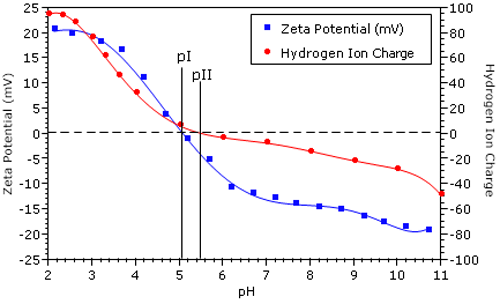
그림 2 는 Zetasizer Nano MPT-2 적정 시스템으로 측정된 100mM NaCl 의 BSA 시료에서 제타전위와 pH 의 결과를 나타낸다. 제로 전기영동도의 pH 로 정의된 등전점(pI = 5.14)은 MPT-2 적정기의 DTS 소프트웨어에 의하여 자동으로 계산되었다. 그림 2 에 100 mM NaCl 용액 의 BSA 에서 분리된 수소이온에 기인하는 총단백질 전하를 덧붙였다. .1 등이온점(pII = 5.5)은 net zero H+ 전하의 pH 로 정의되었다.
|
pl 과 pll 의 차이는 염화이온의 특정흡수를 나타낸다 . 각각의 음염화이온 흡수는 하나의 양전하 아미노산 잔여물과 , 총 중성 단백질 전하를 pH < pll 로 유발시킴으로서 균형을 유지한다 . 1950 년에 Scatchard 등은 멤브레인 분해 실험으로 단백질카운터 이온을 감싸는 정도를 측정했고 염화물이 BSA 를 강하게 감싼다는 것을 발표했다. 2 그림 2 의 결과는 그 결론과 일치함을 보여준다 .
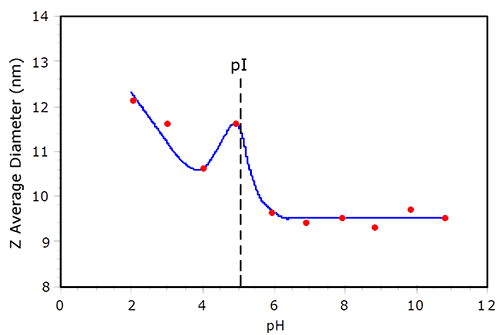
전하를 띤 분자 사이에서의 정전기적반발은 등전점 (pl) 에서 최소화되고 , 미끄럼면에서 총 전하는 0 이다. 반발이 최소화 됨으로써 , 단백질 응집 가능성은 증가한다. 그림 3 에서 보여지는 pl 에서의 단백질 응집 예는, 100mM NaCl 에서 BSA 의 pH 의존량을 보여준다. pH 값이 11 에서 감소 됨으로써, BSA 의 수력학적 크기가 pl 에 가까워 질 때 까지 비교적 일정하다 . pH = 5 (~ pI)일때, 크기의 극대값이 관측된다. pH = 4 일때, 관측된 pl 보다 크기가 작지만 용액의 산성이 증가하면 크기가 커진다 . BSA 에서 중요한 것은 Tanford 등이 보고한 것처럼 적정곡선의 산성부분에서 단백질이 가역팽창을 받는다. pH2 에서의 equivalent hard sphere 지름은 pH > pl 일때 37% 크다. 그림 3 에서 보여지는 것처럼 , pH 가 2 일때 BSA 의 크기는 기본조건보다 30 % 크고, Tanford 등의 결론과 일치한다. 그림 3 에서 보여지는 것처럼 , pH 가 2 일때 BSA 의 크기는 기본조건보다 30 % 크고, Tanford 등의 결론과 일치한다.
|
그림 3 에서의 Z 평균입도는 상관함수의 Cumulants 분석으로부터 얻은 것이다 . Cumulants 분석으로 얻어낸 또 하나의 파라미터는 PdI 또는 분산도 이다 . Cumulants 알고리즘이 우리에게 입도분포를 주지 않는 동안 , PdI 는 상관곡선으로 가상분포 표현의 폭이나 다분산 (Pd) 을 계산할 수 있게 해준다. 표 1 은 100mM NaCl 의 BSA 에서의 복잡분산에 의존하는 pH 의 비교를 보여준다 여기서 본 것처럼 , 적정과정 동한 분산도는 매우 적은 변화를 보인다 . pl 지역을 제외하고 , 제안하고 있는 산성상태에서의 양 증가는 불특정 집합보다는 형태 확장의 결과이다.
| pH | Size (nm) | %Pd |
|---|---|---|
| 10.8 | 9.5 | 45% |
| 9.8 | 9.7 | 48% |
| 8.8 | 9.3 | 46% |
| 7.9 | 9.5 | 46% |
| 6.9 | 9.4 | 45% |
| 5.9 | 9.6 | 47% |
| 4.9 | 11.6 | 58% |
| 4.0 | 10.6 | 48% |
| 3.0 | 11.6 | 47% |
| 2.0 | 12.1 | 47% |
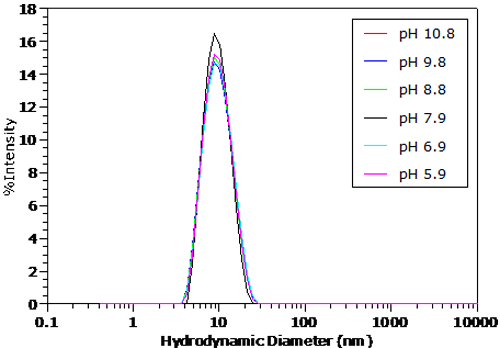
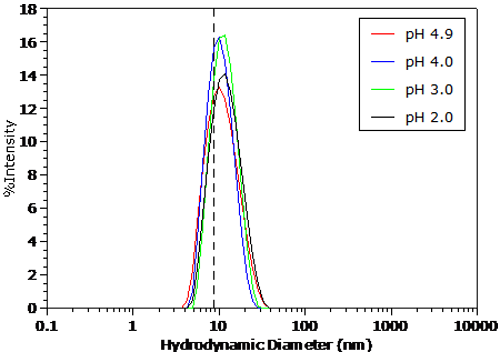
100mM NaCl 에서의 pH 에 따른 BSA 의 입도 분포는 그림 4 와 그림 5 에서 나타난다. 음이 아닌 최소자승 알고리즘을 사용하여 상관함수로 측정한 분포는 변형되었다 . 그림 5 의 점선은 염기 상태에서의 BSA 의 피크점을 나타낸다. pH > pl 경우, 크기분포에서는 현저한 변화가 없음이 관찰되었다 . 그러나, 그림 5 에서처럼 pH < pl 경우에는 Z 평균입도의 결과에서도 알 수 있었듯이, 입도 분포에서도 뚜렷한 증가를 보인다 .
|
|
|
Zetasizer Nano system 과 연동하여 사용하면, Malvern 의 MPT-2 적정기는 연구원의 손끝만으로 완전 자동화가 가능하다. 특별히 약학과 생체분자 응용분야와 관련된 저농도와 저용량의 시료를 필요로 하는 용도로 디자인되었고 , 콜로이드 응용분야에서 필요로 하는 고농도에서도 마찬가지이다 . 시스템은 사용자가 정한 조성 및 농도를 가진 세 개의 적정제를 만들기 위하여 마이크로 실린지를 포함하고 있고, pH, 희석, 첨가제, 전도성 타입 적정의 자동화를 가능하게 하기 위하여 3ml 만큼의 적은 시료량만이 필요하다 .