El cumplimiento normativo es esencial en la industria farmacéutica. Las normas existen a fin de garantizar que solo los productos seguros y efectivos, producidos de manera definida y trazable, lleguen a los consumidores. Sin embargo, garantizar el cumplimiento de estas pautas puede ser estresante y requerir mucho tiempo. Las empresas farmacéuticas deben navegar por un sistema normativo complejo, incluidos los requisitos de la parte 11 de la norma 21 CFR, las pautas de integridad de los datos (ALCOA++) y los estándares de la Farmacopea de los Estados Unidos (USP, por sus siglas en inglés) <1058>, que describe todo el proceso de calificación de instrumentos analíticos.
El cumplimiento normativo es esencial en la industria farmacéutica. Las normas existen a fin de garantizar que solo los productos seguros y efectivos, producidos de manera definida y trazable, lleguen a los consumidores. Sin embargo, garantizar el cumplimiento de estas pautas puede ser estresante y requerir mucho tiempo. Las empresas farmacéuticas deben navegar por un sistema normativo complejo, incluidos los requisitos de la parte 11 de la norma 21 CFR, las pautas de integridad de los datos (ALCOA++) y los estándares de la Farmacopea de los Estados Unidos (USP, por sus siglas en inglés) <1058>, que describe todo el proceso de calificación de instrumentos analíticos.
Las normas de prácticas recomendadas (GxP), incluidos los requisitos de las Prácticas recomendadas de fabricación (GMP/ICH Q7), componen su estructura. Un instrumento debe estar calificado de acuerdo con la especificación de los requisitos del usuario (URS, del inglés User Requirement Specification) del cliente, mediante los procedimientos y la documentación de calificación de instalación (IQ, del inglés Installation Qualification) y calificación de operación (OQ, del inglés Operation Qualification). Luego, el cliente debe realizar pruebas regulares como parte de un programa de calificación de rendimiento (PQ, del inglés Performance Qualification) en curso.
¿Cuáles son los desafíos del cumplimiento?
La realización de mediciones en un entorno validado o regulado necesita más cuidado que nunca. Además del cumplimiento de la parte 11 de la norma 21 CFR, existe un requisito para considerar la integridad de los datos de las mediciones (ALCOA++), incluido el almacenamiento o accesibilidad a largo plazo de los datos, y la calificación del instrumento analítico en sí. En algunos casos, el tiempo que se toma para examinar y aprobar las mediciones puede exceder el tiempo de procesamiento de la muestra. Esto es parte del marco necesario que debe estar implementado en el desarrollo y la fabricación de productos farmacéuticos seguros. Nuestro software, incluido nuestro paquete OmniTrust, permite (con la infraestructura local de TI apropiada) el cumplimiento de la parte 11 de la norma 21 CFR y la orientación sobre la integridad de los datos ALCOA++. Luego, se prueba este cumplimiento mediante auditorías de vigilancia regulares de los organismos reguladores pertinentes.
¿Cómo puede ayudar Malvern Panalytical?
Tenemos amplios conocimientos en esta área, ya que contamos con muchos años de experiencia en instrumentos calificados y en el desarrollo de software que se utiliza en entornos reglamentarios. Además de suministrar necesidades como la OQ o IQ integrales para nuestros productos, nosotros:
- proporcionamos estándares para la calificación de rendimiento (PQ)
- proporcionamos secuencias de comandos de prueba para validar la parte 11 de la norma 21 CFR y las funciones de integridad de datos en su sistema
- proporcionamos un software con muchas funciones que se puede utilizar como una solución que cumpla con la parte 11 de la norma 21 CFR o la integridad de los datos
- podemos entregar una asesoría basada en sus necesidades de validación personalizadas, recomendaciones sobre la calificación farmacéutica (BPF)/ICH Q7 y entregar respaldo con cualquier consulta o requisito adicional
USP <1058>: Calificación de instrumentos analíticos
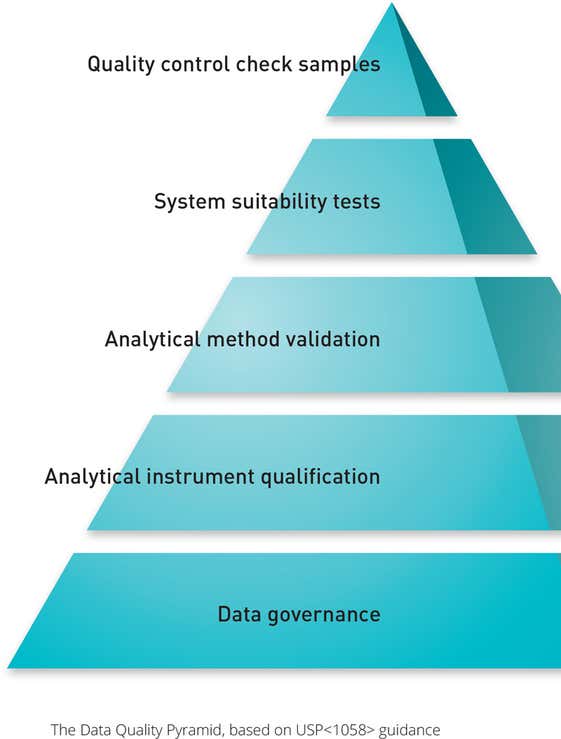
Los requisitos detallados en la USP <1058> resaltan la importancia de las OQ o IQ en el proceso de validación. Estos procedimientos ahora están directamente vinculados con la especificación de los requisitos del usuario (URS) original para un instrumento, junto con su calificación de rendimiento (PQ) y verificación de rendimiento (PV, del inglés Performance Verification).
La calificación de operación también debe probar que el instrumento es adecuado según la aplicación del usuario final y que funciona según el diseño el fabricante.
Malvern Panalytical ofrece un paquete integral de OQ o IQ para este propósito y, también, nos complace consultar sobre las necesidades de pruebas adicionales.
Software para el entorno regulado
La auditoría de una medición puede tomar tiempo, por lo que nuestro software contiene muchas funciones a fin de hacer que este proceso sea más eficiente para nuestros clientes. Se diseñó para ser simple, pero potente, lo que ahorra tiempo en la implementación y en el uso diario, optimiza el flujo de trabajo y permite confiar en que no se encontrarán sorpresas en una auditoría. Esto forma parte de una solución que cumple con la parte 11 de la norma 21 CFR (junto con una política de TI sólida).
A continuación, se incluyen las funciones principales del software:
- Definir roles configurados para los usuarios
- Procesos de aprobación para firmar mediciones
- Registro de las razones para anular mediciones
- Captura de entradas de pistas de auditoría para acciones fallidas debido al uso de credenciales incorrectas
- Auditoría de las funciones de seguridad para una visualización remota
 Descargue el folleto de OmniTrust: la solución de cumplimiento de Malvern Panalytical para el entorno regulado
Descargue el folleto de OmniTrust: la solución de cumplimiento de Malvern Panalytical para el entorno regulado
Servicios de cumplimiento
Estándares
Proporcionamos una variedad de estándares de referencia y calibración para todas sus necesidades de validación.
OQ o IQ y secuencias de comandos de prueba adicionales
Nuestro equipo de Atención al Cliente puede realizar los servicios de OQ o IQ y las secuencias de comandos de prueba para validar la parte 11 de la norma 21 CFR y las funciones de integridad de los datos del software.
Servicios de validación
Siempre recibimos de buena manera las conversaciones con nuestros clientes sobre requisitos de validación adicionales.
Proporcionamos software, incluido nuestro paquete OmniTrust, para su uso en el entorno regulado, que se beneficia de la habilitación de funciones tales como las pistas de auditoría, firmas electrónicas y acceso por capas.
Contenido destacado

Demo at your desk – OmniTrust on Mastersizer 3000; Data integrity solution for the regulated environment
Productos destacados
Rango de equipos Mastersizer

Rango de equipos Zetasizer