Já utilizados extensivamente para a atividade local, os OINDPs também mostram grande promessa para o fornecimento sistêmico efetivo de uma variedade de terapias. Aceitabilidade do paciente, absorção rápida, prevenção do trato gastrointestinal e a oportunidade de diferenciação do produto são apenas alguns dos fatores motivadores.
Ao desenvolver inaladores ou sprays, o desenvolvimento da formulação e do dispositivo caminham juntos. As alterações feitas em um afetarão o outro e vice-versa. Como exemplo, o projeto e a geometria de um bico de pulverização afetam a tensão na suspensão e, portanto, a distribuição das gotas de pulverização. Da mesma forma, uma mudança de excipiente pode afetar a viscosidade da formulação e a eficiência com que ela pode ser bombeada através do bico de pulverização — isso é fundamental, pois a distribuição do tamanho da gota influencia onde o medicamento é depositado no trato respiratório e, portanto, também afeta sua biodisponibilidade e velocidade de ação.
As soluções de análise físico-química da Malvern Panalytical ajudam você a entender o impacto de suas decisões na formulação e no processo sobre o medicamento final, orientando você para o sucesso.
Caracterização e seleção do excipiente de formulação

Ao escolher seus excipientes, há uma série de considerações que podem afetar sua formulação ou mesmo seu produto de medicamento final. Excipientes como polímeros são frequentemente usados para modular a viscosidade de uma suspensão ou solução. Por isso, muitas vezes eles podem influenciar na facilidade de bombeamento ou no processamento da suspensão, e em sprays nasais ou nebulizadores podem afetar diretamente a distribuição do tamanho das gotas do spray. A distribuição do tamanho das partículas de transporte de medicamentos, como a lactose em inaladores de pó seco, é essencial para a administração do medicamento aos pulmões, e às vezes a forma dos excipientes e das partículas API pode afetar a forma como elas interagem e fluem durante o processamento.
A Malvern Panalytical tem várias ferramentas que são comumente usadas para a análise de ingredientes ou matérias-primas de diferentes fornecedores e também podem ser aplicadas para determinar se lotes diferentes são iguais ou mostram diferenças.
Saiba mais sobre a caracterização do excipiente
Pharmaceutical Excipient Characterization
Nossas soluções para caracterização e seleção de excipientes

OMNISEC
Linha Mastersizer
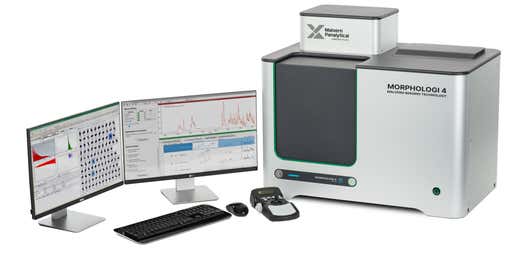
Morphologi 4-ID
Análise da estabilidade do API em todo o desenvolvimento de formulação e processo

Estudos de degradação acelerados de API e excipientes
A difração de pó de raios X fornece uma visão exclusiva das alterações na forma de cristal de medicamentos, tamanho e morfologia de cristalito, bem como alterações feitas nas proporções entre o amorfo e o cristalino do API na formulação durante estudos de tensão acelerados para avaliar ou otimizar a estabilidade da formulação.
Desenvolvimento de processos e monitoramento de processos
Nossas ferramentas de caracterização físico-química são usadas para avaliar a estabilidade de APIs e excipientes em uma formulação, em todas as condições de processamento, para garantir que os parâmetros do processo sejam controlados e otimizados de forma que o produto final do medicamento atenda aos CQAs (Critical Quality Attributes, Atributos de qualidade críticos) necessários.
Conteúdo em destaque
Automatic condensation-free combined temperature-humidity control for XRD studies

XRD Masterclass 2: In situ Stability Studies
Crystallite size determination of a pharmaceutical compound by Rietveld analysis

Crystallinity determination - Quantification of low amounts of amorphous material in a crystalline matrix and vice versa

What are the targeting methods used in solid form analysis?
The influence of electrostatic stabilisation in apolar suspension formulations.
Produtos em destaque

Variedades do Empyrean
Epsilon 1 para a indústria farmacêutica

Morphologi 4-ID
Estudos de comparabilidade — para apoiar o processo, formulação ou alterações materiais e estudos de bioequivalência in vitro

Em qualquer processo, podem ser necessárias alterações. Na indústria farmacêutica, exemplos podem incluir uma mudança no fornecedor de um excipiente ou API, uma mudança de uma peça de máquina, uma movimentação de um produto entre locais de fabricação ou uma pequena mudança na composição da formulação. Todas essas alterações devem ser controladas para que não afetem o medicamento final.
As soluções físico-químicas da Malvern Panalytical são usadas regularmente para ajudar na avaliação de comparabilidade para verificar se há alterações em um produto quando houve uma mudança no processo usado para criá-lo. Além disso, nossas tecnologias também são usadas para mostrar bioequivalência in vitro entre produtos de referência e de teste quando os genéricos estão sendo desenvolvidos. Este teste pode provar que a combinação de produto genérico e dispositivo fornece o mesmo medicamento da mesma forma que o produto inovador, o que pode reduzir drasticamente a quantidade de testes clínicos necessários e acelerar a passagem de um produto farmacêutico genérico para o mercado.
Conteúdo em destaque
Component specific particle sizing in orally inhaled and nasal drug products (OINDPs)
Supporting dry powder inhaler formulation development using component-specific particle characterization
In vitro bioequivalence studies for a metered dose inhaler formulation using the Morphologi automated particle imaging system
Rapid Generic Pharmaceutical Product Development
Achieving Bioequivalence in Generic Formulations by Characterizing Particle Size, Shape & Chemical Identity
Soluções em destaque

Morphologi 4-ID

Variedades do Empyrean
Otimizando o desempenho do dispositivo e da formulação
Conteúdo em destaque
Laser diffraction and imaging - complementary techniques for nasal spray development
Consistency of Delivery is Key in Nasal Spray Treatments
Enhancing the in vitro assessment of nasal sprays
Soluções em destaque







